Ведутся технические работы. Это может временно повлиять на скорость работы сайта. Приносим извинения за неудобства и благодарим за ваше понимание!
Ведутся технические работы. Это может временно повлиять на скорость работы сайта. Приносим извинения за неудобства и благодарим за ваше понимание!
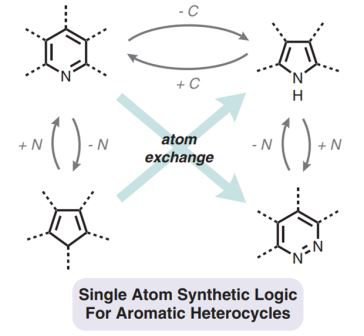
Американские химики разработали фотохимическую реакцию, с помощью которой можно превращать шестичленные азотные гетероциклы в пятичленные. Замещенные N-оксиды хинолинов в две стадии превратились в замещенные индолы. Такая реакция позволит упростить синтез биологически активных соединений.
 Изменять скелет ароматических гетероциклов можно с помощью удаления и введения отдельных атомов
Изменять скелет ароматических гетероциклов можно с помощью удаления и введения отдельных атомов
© M. Levin et al. / Science, 2022
Когда химики тестируют вещества на биологическую активность, им часто приходится получать десятки похожих молекул. Небольшое изменение в углеродном скелете молекулы может привести к повышению биологической активности. Поэтому химики планируют синтез так, чтобы некоторые фрагменты было удобно варьировать. В этом, например, сильно помогают реакции кросс-сочетания: одну бороновую кислоту можно ввести в реакцию с разными галогенидами и получить несколько похожих соединений.
Но варьировать заместители в молекуле намного проще, чем изменить ее основной углеродный скелет. Часто он состоит из устойчивых ароматических фрагментов, которые получаются на ранней стадии синтеза. И если вдруг оказывается, что один ароматический фрагмент подходит для биологических испытаний больше, чем другой, ученым приходится проводить синтез с самого начала.
Чтобы изменять скелет молекулы стало легче, химики под руководством Марка Левина (Mark D. Levin) из Чикагского университета занялись разработкой реакций, с помощью которых из ароматических гетероциклов можно удалять отдельные атомы. Такие реакции позволяют превращать одни гетероциклы в другие на поздних стадиях синтеза, при этом не нужно начинать синтез заново.
Химикам было известно, что N-оксиды хинолинов могут под действием света ртутной лампы перегруппировываться в неустойчивые бензокcазепины, а те, в свою очередь, превращаться в индолы под действием кислоты. Но проблема заключалась в том, что фотохимическая перегруппировка работает далеко не для всех хинолинов и чаще всего приводит к трудно разделяемой смеси продуктов.
Ученые предположили, что если облучать реакционную смесь светом с определенной длиной волны, перегруппировка будет проходить более чисто. Они взяли раствор N-оксида 2-метилхинолина в бензоле и облучали его светом с длиной волны 395 нанометров. Через пять часов реакции выход бензоксазепина составил 91 процент. Когда в реакционную смесь добавили трифторуксусную кислоту, с выходом 78 процентов получился N-ацетилиндол, как и ожидали ученые.
Чтобы показать, какие хинолины можно использовать в реакции, химики протестировали 39 разных субстратов. Оказалось, что реакция чувствительна к заместителю во втором положении хинолина: гетероатомы и третичные алкильные фрагменты в этом положении не позволили получить нужные продукты. Большая часть других замещенных хинолинов успешно превратилась в соответствующие индолы.
Далее химики показали, что их реакцию можно проводить в проточном реакторе, используя граммовые загрузки реагентов. Так, 2-фенил-3-метилхинолин превратился в один грамм замещенного индола за 30 минут с выходом в 77 процентов.
В результате авторам удалось подобрать условия, в которых ароматические хинолины превращались в индолы. Вместе с уже известными способами введения и удаления атомов, новый метод позволяет легко изменять основной скелет молекулы. Это химики показали на примере 2-фенил-3-метилхинолина, из которого с помощью удаления двух атомов углерода и введения атомов углерода и азота удалось получить хинолин с другим порядком заместителей, два различных индола и 3-фенилциннолин.
 С помощью удаления и введения отдельных атомов химикам удалось получить четыре разных гетероцикла
С помощью удаления и введения отдельных атомов химикам удалось получить четыре разных гетероцикла
© M. Levin et al. / Science, 2022
Статья опубликована в журнале Science
Источник: Михаил Бойм nplus1.ru
| ( ! ) Warning: Invalid argument supplied for foreach() in /home/domains/malitikov.ru/public_html/wp-content/themes/malitikov/single.php on line 44 | ||||
|---|---|---|---|---|
| Call Stack | ||||
| # | Time | Memory | Function | Location |
| 1 | 0.0000 | 350088 | {main}( ) | .../index.php:0 |
| 2 | 0.0000 | 350368 | require( '/home/domains/malitikov.ru/public_html/wp-blog-header.php ) | .../index.php:17 |
| 3 | 0.1934 | 8880808 | require_once( '/home/domains/malitikov.ru/public_html/wp-includes/template-loader.php ) | .../wp-blog-header.php:19 |
| 4 | 0.1951 | 8912392 | include( '/home/domains/malitikov.ru/public_html/wp-content/themes/malitikov/single.php ) | .../template-loader.php:132 |